Neue Trends in der Pathologie (Teil 1)
Verfasst von Ilgar Guseinov am 29.11.2022
In Artikeln und offiziellen Gesellschaften finden sich zahlreiche Definitionen der "Digitalen Pathologie", aber jede davon ist richtig und falsch gleichzeitig. Einige sind zu kurz gefasst und erlauben es nicht, das gesamte Bild dahinter zu sehen, während andere diesen Bereich nur als ein Werkzeug im Dienste eines bereits bestehenden Medizinbereichs sehen. Beschränken wir uns daher vorerst auf die folgende Definition, damit sie für diejenigen, die sich mehr für die Computerwissenschaft interessieren, verständlich ist und die Experten auf diesem Gebiet nicht verärgert werden.
Digitale Pathologie ist die Praxis der Pathologie, bei der hochauflösende digitale Bilder anstelle des Okulars eines herkömmlichen Mikroskops zur Untersuchung von Gewebe- oder Flüssigkeitsproben verwendet werden.
In diesem und den folgenden Artikeln werden wir diese Definition erweitern und erläutern, wie das med4PAN-Projekt das Versorgungsniveau mit 5G-Technologien verbessert.
Doch bevor wir zu den digitalen Bildern selbst kommen, wollen wir uns die Infrastruktur eines typischen digitalen Pathologielabors ansehen. Natürlich können wir gleich mit der digitalen Bildgebung und -verarbeitung beginnen, aber das allein macht noch nicht viel Sinn.
Digitaler Arbeitsablauf
In jedem Pathologielabor, ob digital oder traditionell, laufen die gleichen Prozesse ab, aber die Digitalisierung drückt jedem Schritt ihren Stempel auf.
Annahme eines Probenmaterials
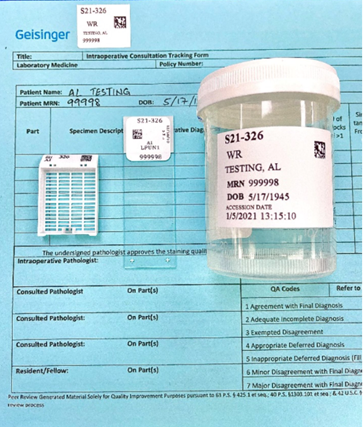
Obwohl diese Stufe recht einfach klingt, hängt viel von ihrer Qualität ab. Ziel dieser Phase ist es, die präanalytischen Faktoren zu reduzieren, die die Qualität der Slides und des Bildes und damit das Ergebnis beeinflussen können. Die Intaktheit des Behältnisses, in dem die Probe angekommen ist, die Angemessenheit der Informationen in den Begleitdokumenten, das Vorhandensein von Kontaktinformationen und die Konsistenz der Dokumente und des Inhalts sind sehr wichtige Informationen, die vor der Eingabe dieser Daten in das Laborinformationssystem (LIS) geklärt werden sollten. Hier ist es auch notwendig, alle Papierdokumente loszuwerden und alle Daten (so weit wie möglich) in das LIS einzugeben. Nach der Eingabe aller Daten erhält die Probe einen eindeutigen Zahlencode und einen QR-Code, da sie sonst nicht weiter durch das Labor geleitet werden kann.
Bild 1. Vergleich von modernen Beschriftungen und handschriftlichen Kennzeichnungen von Kassetten und Präparaten. [1]
Bild 2. Beispiele für barcodierte Papieranforderung, Probenbehälter, Kassettengravur-Etikett und Objektträger-Etikett. [2]
Erfahren Sie hier mehr über das Barcoding Tracking System: https://www.pathologyoutlines.com/topic/informaticsbarcodingtracking.html
Ein Laborinformationssystem (LIS) ist eine Softwareanwendung oder Datenbank, die zur Verwaltung, Speicherung und Analyse der in einem Labor erzeugten Daten verwendet wird. Es ist eine kritische Komponente des Betriebs eines Labors, da es die Genauigkeit, Integrität und Sicherheit der gesammelten und analysierten Daten gewährleistet.
Zu den wichtigsten Funktionen eines Laborinformationssystems gehören:
Datenverwaltung: Ein LIS kann dazu verwendet werden, alle in einem Labor anfallenden Daten zu speichern, zu organisieren und zu verwalten, einschließlich Testergebnisse, Patienteninformationen, Gerätekalibrierungsprotokolle und vieles mehr. Auf diese Weise kann sichergestellt werden, dass die Daten genau aufgezeichnet werden und für Analysen und Berichte leicht zugänglich sind.
Qualitätskontrolle: Mit einem LIS können Qualitätskontrollmaßnahmen durchgeführt werden, wie z. B. automatische Prüfungen auf Fehler oder Werte außerhalb des zulässigen Bereichs, um die Genauigkeit und Zuverlässigkeit der Daten zu gewährleisten.
Berichterstattung: Ein LIS kann Berichte und andere Arten von Datenausgaben erstellen, die für verschiedene Zwecke verwendet werden können, z. B. für die Qualitätssicherung, die Einhaltung von Vorschriften oder für Forschung und Entwicklung.
Integration: Ein LIS kann mit anderen Systemen und Software, wie z. B. elektronischen Krankenakten, integriert werden, um den Informationsaustausch zu erleichtern und den Arbeitsablauf zu verbessern.
Insgesamt kann ein Laborinformationssystem die Effizienz und Effektivität der Abläufe in einem Labor erheblich verbessern und ist ein unverzichtbares Instrument für jede Organisation, die auf datengestützte Entscheidungsfindung angewiesen ist.
Erfahren Sie mehr über LIS hier: https://www.youtube.com/watch?v=uVz25xKRcYw
Zuweisung und Priorisierung der Proben
Anschließend werden die registrierten und beschrifteten Proben an das Labor geliefert, wo sie sortiert (z. B. nach Komplexität) oder nach Dringlichkeit priorisiert werden können und dann an die Abteilung.
Makroskopische Untersuchung
Der Prozess der Sektion (makroskopische Untersuchung) zielt darauf ab, das Makropräparat zu beschreiben und die Bereiche von Interesse zu finden und hervorzuheben, die in den Kassetten weitergeführt werden. Dies ist eine der wichtigsten Phasen des gesamten Prozesses. Fehler in dieser Phase können zum Verlust von Bereichen führen, die wichtige Fragen beantworten können.
Bild 3. Ein Beispiel für eine Grossing-Station. 1 - Kamera; 2 - Touchscreen-Monitor; 3 - Mikrofon; 4 - Profilhalterung; 5 - Tisch- und Komponentensteuerungspedale [3]
Im Vergleich zum traditionellen Arbeitsplatz eines Pathologen weist der moderne Arbeitsplatz eine Reihe von Unterschieden auf. Nach Erhalt einer Probe scannt ein Spezialist den QR-Code mit einem Lesegerät ein, und der automatisch im LIS registrierte Fall wird auf dem Monitor angezeigt. Eine über der Arbeitsstation angebrachte Kamera ermöglicht es, Fotos zu machen und die Parameter der Probe zu fixieren. Diese Daten werden sofort auf einen lokalen Server hochgeladen und mit dem aktuellen Fall im LIS verknüpft. Während der makroskopischen Untersuchung kann ein Mikrofon verwendet werden, um das Untersuchungsprotokoll aufzuzeichnen.
Ein Beispiel für den Schritt der makroskopischen Untersuchung sehen Sie hier
https://www.youtube.com/watch?v=W-YS87ZJHM0
Verarbeitung
Der Verarbeitungsschritt im Labor unterscheidet sich nicht wesentlich von dem in einem normalen Labor. Aber auch hier sind die Prozesse entsprechend den Leitlinien hoch automatisiert.
Einbetten
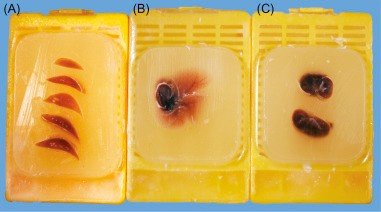
Nachdem die erforderlichen Messungen und Beschreibungen vorgenommen wurden, werden die Proben in Kassetten gelegt und zur Fixierung mit Paraffin gefüllt. Nach dem Abkühlen erhält man einen (histologischen) Paraffinblock (Abb.4). Auf diese Weise kann das Präparat für lange Zeit aufbewahrt werden.
Bild 4. In Paraffin eingebettetes Gewebe [4]
Dies ist im Video deutlich zu sehen: https://www.youtube.com/watch?v=xIyXA3c3oxU
Schneiden
Um Objektträger aus den in Paraffin fixierten Geweben zu erhalten, müssen diese in dünne Scheiben geschnitten werden. Dies geschieht mit einer Maschine, die Mikrotom genannt wird (siehe Video). Nach dem erfolgreichen Schneiden wird der Schnitt auf einen Objektträger aufgetragen, fixiert und zur Färbung eingeschickt.
https://www.youtube.com/watch?v=XDoTLJ3ZXtY
Färben und Einbetten
Um die Mikrostrukturen des Gewebes besser sichtbar machen und beurteilen zu können, ist es notwendig, sie zu färben. Routinemäßig wird die H&E-Färbung (Hämatoxylin und Eosin) verwendet - Hämatoxylin färbt Strukturen, die DNA und RNA enthalten (Zellkern, Ribosomen und RNA-reiche Teile des Zytoplasmas), und Eosinophil färbt das Zytoplasma und seine Strukturen. Darüber hinaus gibt es eine große Anzahl von Färbungen zur Identifizierung verschiedener Zellstrukturen. Heute ist der Färbeprozess vollständig automatisiert. https://www.youtube.com/watch?v=6-WOgY5-P04
Jetzt sind die Dias bereit zum Scannen und Untersuchen, aber dazu mehr im nächsten Beitrag!
Referenzen:
[1] Brown, R. W., Speranza, V. D., Alvarez, J. O., Eisen, R. N., Frishberg, D. P., Rosai, J., ... & Thomas, N. E. (2015). Uniform labeling of blocks and slides in surgical pathology: Guideline from the college of American Pathologists Pathology and Laboratory Quality Center and the National Society for Histotechnology. Archives of Pathology & Laboratory Medicine, 139(12), 1515-1524
[2] Absar, F., & Prichard, W. (2022, March 7). Barcoding and tracking. https://www.pathologyoutlines.com/topic/informaticsbarcodingtracking.html
[3] https://www.milestonemedsrl.com
[4] Treuting, P. M., Dintzis, S., & Montine, K. S. (Eds.). (2017). Comparative anatomy and histology: a mouse, rat, and human atlas. Academic Press.